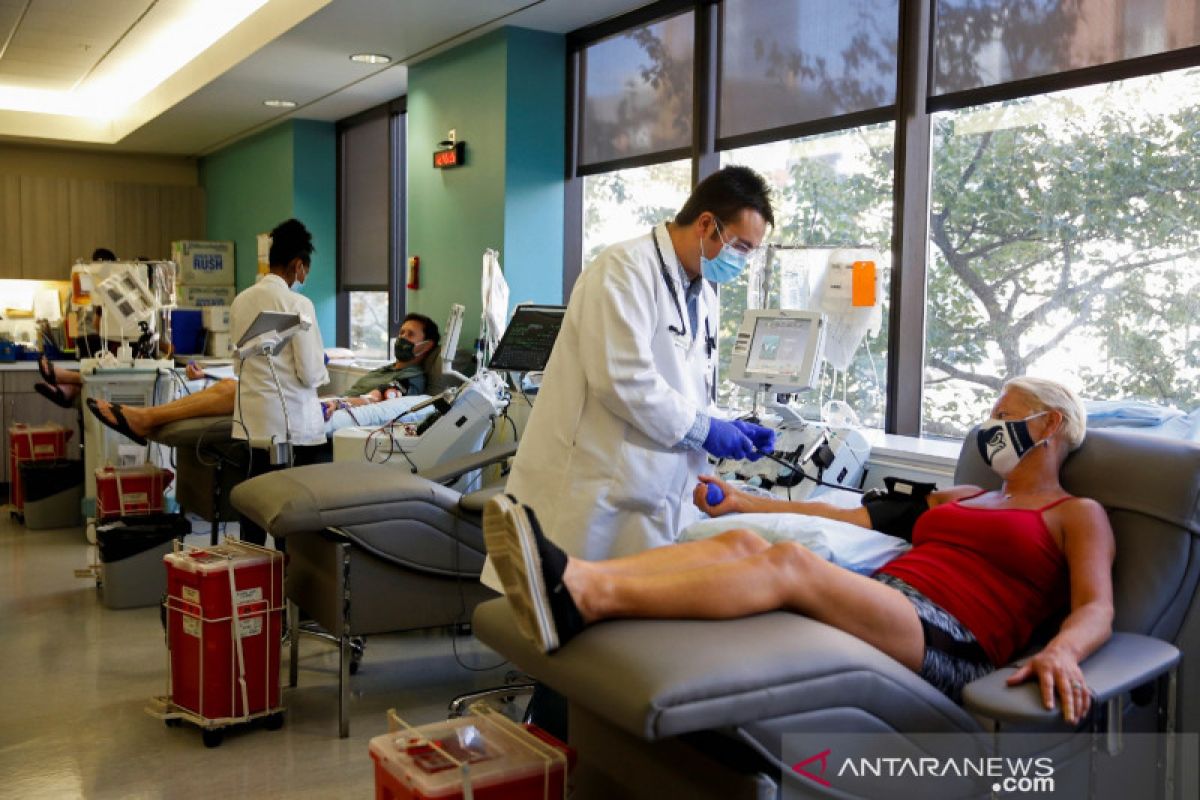
New York (ANTARA) - Grup Takeda Pharmaceutical, yang mengembangkan obat COVID-19 dari plasma darah, mulai melakukan produksi sambil uji klinis tahap tiga menentukan keampuhan obat tersebut, menurut CEO Takeda Christophe Weber pada Senin (12/10) .
Grup itu, yang dikenal CoVIg Plasma Alliance, mendaftarkan pasien pertamanya dalam uji klinis Tahap 3 pada Jumat setelah tertunda selama berbulan-bulan. Pihaknya berencana mendaftarkan 500 pasien dewasa dari Amerika Serikat, Meksiko serta 16 negara lainnya dan berharap mendapatkan hasilnya akhir tahun ini.
"Peluang untuk berhasil sangat tinggi," kata Weber saat wawancara. "Dan itulah alasannya kami meluncurkan kampanye agar mempercepat donasi plasma konvalesen untuk membuat sekaligus memproduksi produk ini."
Baca juga: China laporkan kasus lokal COVID-19 pertama setelah 2 bulan
Aliansi, yang terdiri atas CSL Behring, Biotest AG Jerman dan perusahaan lainnya, sedang menguji terapi globulin hiperimun yang berasal dari plasma darah pasien sembuh COVID-19. Terapi globulin hiperimun menghasilkan dosis antibodi standar dan tidak perlu dibatasi pada pasien dengan kecocokan jenis darah.
Itu membuatnya lebih berkembang dan mudah ketimbang pengobatan dengan plasma konvalesen yang diambil dari pasien sembuh.
Baca juga: Kasus positif COVID-19 di Indonesia 3.267 orang, sembuh 3.492 orang
Proses produksinya mahal.
Menurut Weber, pengobatan tersebut bisa saja sedikit lebih mahal dari obat antibodi monoklonal seperti yang dikembangkan Regeneron Pharmaceuticals dan Eli Lilly and Co. Aliansi tidak bermaksud mengambil keuntungan dari pengobatan tersebut, katanya.
CEO Takeda mengaku tidak mengetahui jumlah dosis obat yang mampu dihasilkan oleh grup tersebut pada akhir tahun ini. Itu tergantung pada donasi serta ukuran dosis yang mereka tetapkan dalam uji klinis.
Uji klinis tersebut akan menguji terapi globulin hiperimun yang digabungkan dengan obat antivirus remdesivir milik Gilead Sciences dibandingkan dengan pasien yang mengonsumsi remdesivir saja, katanya.
Sumber: Reuters