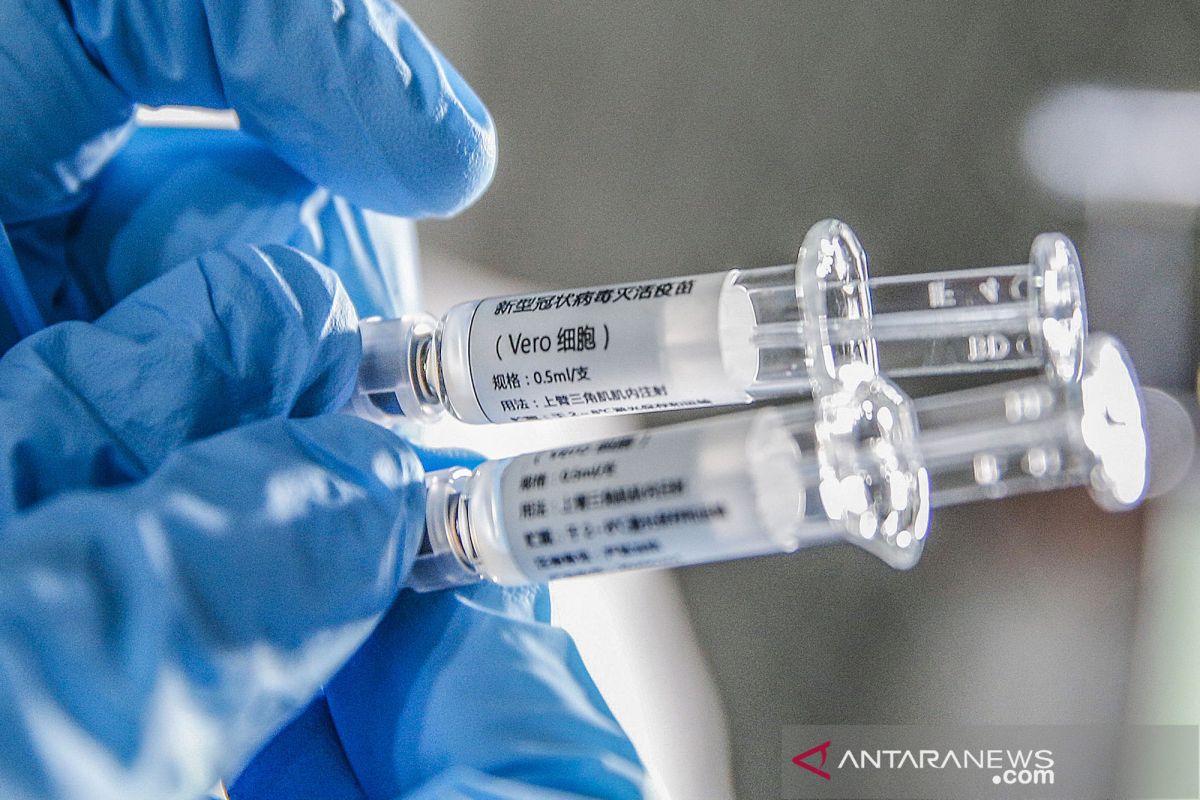
Jakarta (ANTARA) - Indonesia telah mendaftar untuk mengikuti program uji coba global (solidarity trial) untuk vaksin COVID-19 yang dikoordinasi oleh Organisasi Kesehatan Dunia (WHO), kata koordinator nasional WHO di Indonesia, Irmansyah, Jumat (15/5).
"WHO akan menyusun protokol (mengenai uji coba vaksin, red), rasanya sudah final, nanti akan disebarkan. Kita sudah mendaftarkan diri untuk solidarity trial vaccine ini," kata Irmansyah yang juga menjabat sebagai Kepala Pusat Penelitian dan Pengembangan Sumber Daya dan Pelayanan Kesehatan Kementerian Kesehatan Republik Indonesia.
Menurut dia, sebagaimana uji coba obat-obatan COVID-19, solidarity trial untuk vaksin bertujuan mempercepat proses pemeriksaan dan penentuan vaksin untuk penyakit akibat virus corona jenis baru (SARS-CoV-2). Umumnya, proses pengembangan vaksin butuh waktu sekitar belasan tahun, sementara saat penentuan vaksin Ebola, peneliti membutuhkan waktu kurang lebih empat tahun, terang Irmansyah.
"COVID-19 ini (ditemukan, red) mungkin akhir tahun lalu, dan (virus, red) berhasil diisolasi mungkin awal tahun ini atau akhir tahun lalu, dan (vaksin, red) itu sudah ditargetkan tidak lebih dari satu tahun atau tahun ini. Itu percepatan yang luar biasa, sangat menjanjikan," ujar Irmansyah dalam seminar virtual yang diadakan oleh Kementerian Luar Negeri RI di Jakarta.
WHO, lewat laman resminya, menyebutkan saat ini ada sekitar 120 vaksin yang telah diusulkan dari berbagai negara di dunia untuk COVID-19. Namun, hanya enam vaksin yang telah memasuki uji klinis dan 70 lainnya masih menjalani evaluasi praklinis. Uji klinis merupakan tahapan vaksin dapat diuji coba ke manusia.
Menurut dokumen yang disusun WHO, beberapa vaksin telah digunakan untuk penyakit sejenis seperti MERS, SARS, Influenza, Tuberkulosis, dan beberapa penyakit lain, seperti Ebola, Chikungunya, Zika, MenB, Flu A, Hepatitis C, dan H7N9.
Merujuk pada dokumen yang sama, produsen vaksin merupakan perusahaan bioteknologi dan institut yang beberapa di antaranya berasal dari China, Inggris, Amerika Serikat, Swedia, Jepang, Kanada, Italia, India, Jerman, Spanyol, dan Rusia.
Sementara di Indonesia, salah satu badan usaha milik negara, PT Bio Farma, juga berupaya mengembangkan vaksin dengan bekerja sama dengan lembaga riset dalam negeri melalui konsorsium nasional Kementerian Riset dan Teknologi/BRIN (Badan Riset dan Inovasi Nasional), Pusat Penelitian dan Pengembangan Kesehatan Kementerian Kesehatan RI, Badan Pengkajian dan Pengembangan Teknologi (BPPT), Lembaga Eikjman, serta lembaga riset luar negeri, kata Direktur Operasi PT Bio Farma, M Rahman Roestan, pada sesi seminar yang sama.
"(Salah satu, red) pendekatan untuk pengembangan vaksin COVID-19 ini yang pertama adalah mencari partner (mitra, red) dari luar negeri untuk mendapatkan transfer teknologi. Kita bekerja sama dengan institut riset, salah satunya dengan CEPI (Koalisi untuk Inovasi Persiapan Epidemi) di Norwegia. Kita juga cari yang sudah siap, salah satunya manufacturer (produsen vaksin, red) di China," kata Rahman ketika menjelaskan langkah jangka pendek pengadaan vaksin di Indonesia.